07/05/2017
El cloruro de sodio (NaCl), comúnmente conocido como sal de mesa, presenta una estructura cristalina maravilloso que ha sido objeto de estudio durante siglos. Su representación gráfica requiere entender su compleja disposición atómica a nivel microscópico, la cual se traduce en propiedades macroscópicas como su sabor salado y su capacidad para disolverse en agua.

Estructura cristalina del NaCl
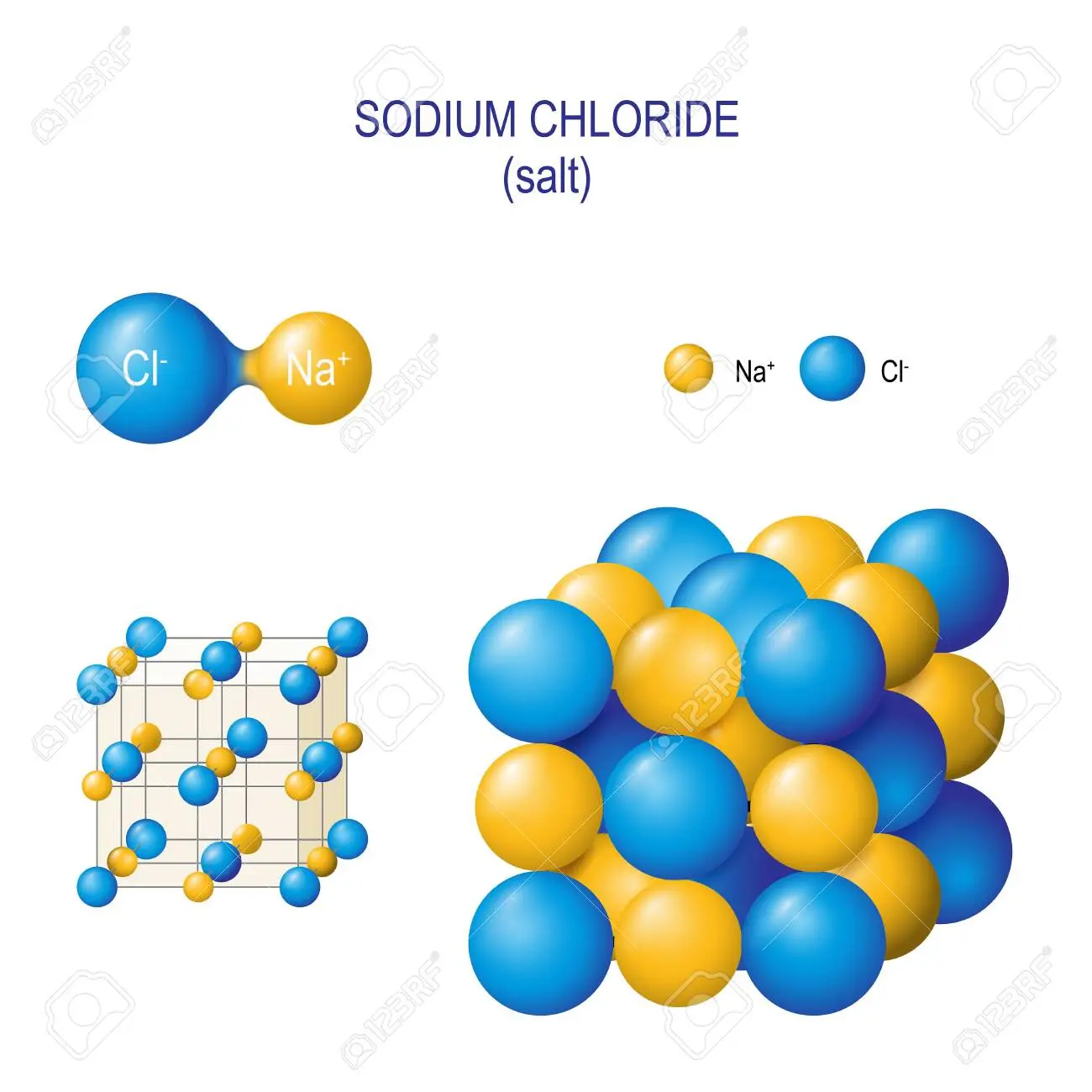
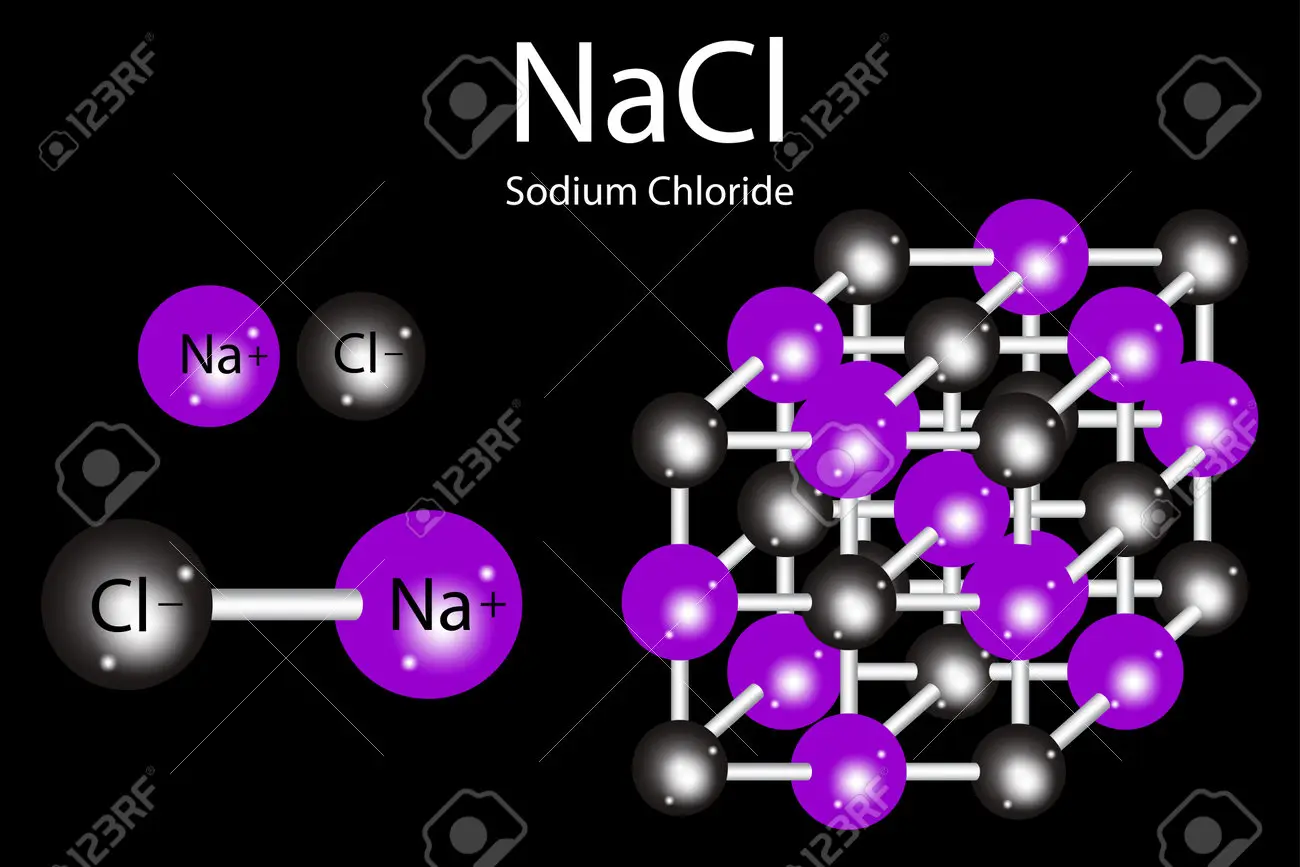
La estructura del NaCl se caracteriza por su celda unitaria cúbica centrada en las caras (ccc). Esta celda unitaria es la unidad básica que se repite para formar el cristal completo. Dentro de esta celda, los iones de sodio (Na+) y los iones de cloruro (Cl-) se alternan de manera regular. No se trata de moléculas de NaCl individuales, sino de una red tridimensional de iones unidos por fuerzas electrostáticas.
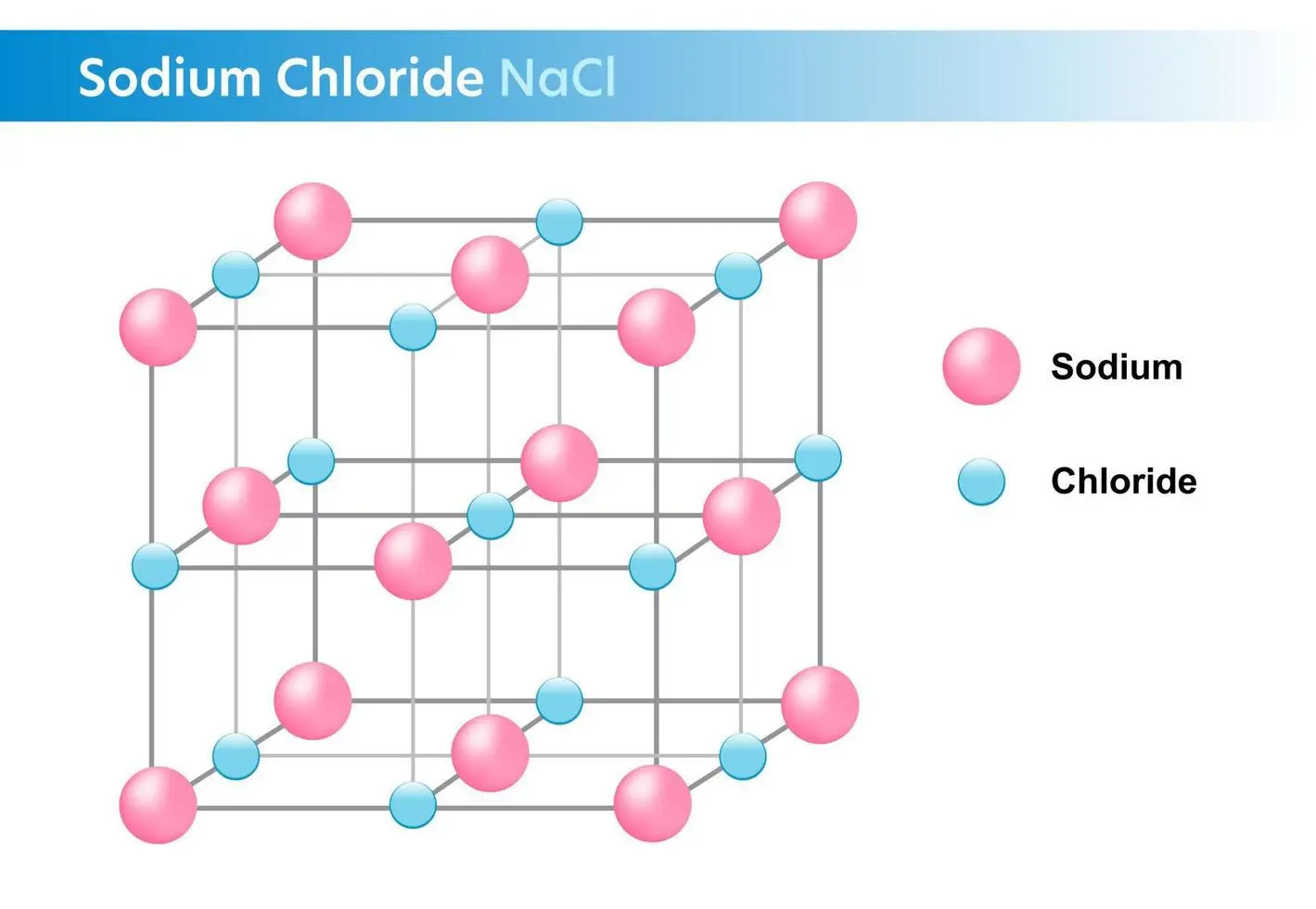
Una forma de visualizarlo es imaginar un cubo. En los vértices, en el centro de cada cara y en el centro del cubo se encuentran los iones, alternando Na+ y Cl-. Cada ion Na+ está rodeado por seis iones Cl-, y cada ion Cl- está rodeado por seis iones Na+. Esta disposición crea una estructura estable y eficiente en términos de empaquetamiento.
Posiciones de los iones en la celda unitaria
Para comprender mejor la disposición atómica, es útil analizar las diferentes posiciones que ocupan los iones dentro de la celda unitaria:
- Posición central única: Un ion ocupa el centro de la celda unitaria.
- Sitios de cara: Los iones se ubican en el centro de cada una de las seis caras del cubo.
- Sitios de borde: Los iones se sitúan en el medio de cada uno de los doce bordes del cubo.
- Sitio de esquina: Los iones se encuentran en cada uno de los ocho vértices del cubo.
Contando los iones de manera apropiada (considerando que los iones en las caras, bordes y esquinas son compartidos por varias celdas unitarias), se determina que hay la misma cantidad de iones Na+ y Cl- en la celda unitaria, manteniendo la neutralidad eléctrica del cristal.
Representaciones alternativas
Existen diferentes maneras de representar la estructura del NaCl, dependiendo del enfoque y el nivel de detalle deseado:
- Modelo de esferas y barras: Este modelo utiliza esferas de diferente tamaño (generalmente, Na+ más pequeño que Cl-) para representar los iones, y barras para representar los enlaces iónicos. Este modelo es útil para visualizar la disposición espacial de los iones.
- Modelo de empaquetamiento compacto: Este modelo enfatiza la disposición de los iones en capas, mostrando cómo se empaquetan los aniones (Cl-) para formar una estructura compacta, y cómo los cationes (Na+) ocupan los huecos entre los aniones.
- Diagramas bidimensionales: Se utilizan diagramas bidimensionales simplificados para mostrar la disposición alternada de los iones en planos seleccionados. Aunque no representan la tridimensionalidad completa de la estructura, son útiles para ilustrar el patrón de repetición.
Importancia de la representación gráfica
La representación gráfica del cloruro de sodio es crucial para comprender sus propiedades físicas y químicas. La estructura cristalina determina:
- Propiedades físicas: Punto de fusión, punto de ebullición, dureza, solubilidad.
- Propiedades químicas: Reactividad, capacidad de conducir electricidad (cuando está disuelto en agua).
La comprensión de esta estructura es fundamental en diversos campos, incluyendo la química, la cristalografía, la ciencia de materiales y la biología.
Comparativa con otras estructuras cristalinas
| Compuesto | Estructura cristalina | Características |
|---|---|---|
| Cloruro de sodio (NaCl) | Cúbica centrada en las caras | Iones de Na+ y Cl- alternándose en una red cúbica. |
| Cloruro de cesio (CsCl) | Cúbica centrada en el cuerpo | Ion Cs+ en el centro de un cubo con iones Cl- en los vértices. |
| Diamante | Cúbica de diamante | Red tetraédrica de átomos de carbono. |
La tabla ilustra que la estructura cristalina varía significativamente entre compuestos iónicos, dependiendo del tamaño y la carga de los iones involucrados. La representación gráfica permite la comparación visual de estas diferentes estructuras.
Consultas habituales sobre la representación gráfica del NaCl
Algunas de las preguntas más frecuentes sobre la representación gráfica del cloruro de sodio incluyen:
- ¿Cómo se representa la celda unitaria del NaCl?
- ¿Qué tipo de enlace se representa en la estructura del NaCl?
- ¿Cuál es la diferencia entre la representación de esferas y barras y el modelo de empaquetamiento compacto?
- ¿Cómo se puede visualizar la estructura tridimensional del NaCl a partir de una representación bidimensional?
Responder estas preguntas con precisión y claridad requiere una comprensión profunda de la estructura cristalina del cloruro de sodio y sus métodos de representación.
La representación gráfica del cloruro de sodio es un aspecto fundamental para comprender su estructura, propiedades y comportamiento a nivel atómico y macroscópico. El uso de diferentes modelos y técnicas de representación permite una comprensión más completa de este compuesto tan común y esencial.