29/10/2016
El diagrama P-V, también conocido como diagrama de presión-volumen, es una herramienta gráfica fundamental en termodinámica que representa la relación entre la presión (P) y el volumen (V) de un sistema, generalmente un gas. Su utilidad radica en la capacidad de visualizar procesos termodinámicos y calcular el trabajo realizado durante esos procesos. Comprender cómo se grafica y cómo interpretar la información que proporciona es esencial para cualquier estudiante o profesional de la ingeniería, física o química.

Graficando un diagrama P-V: Pasos y Consideraciones
La construcción de un diagrama P-V es relativamente sencilla. Se utilizan dos ejes cartesianos: el eje horizontal (abcisa) representa el volumen (V), generalmente en unidades como litros (L) o metros cúbicos (m³), y el eje vertical (ordenada) representa la presión (P), medida en atmósferas (atm), pascales (Pa) o otras unidades de presión. Cada punto en el gráfico representa un estado termodinámico específico del sistema, definido por un valor particular de presión y volumen.
Para graficar un proceso termodinámico en un diagrama P-V, se necesita información sobre cómo cambian la presión y el volumen a lo largo del proceso. Esta información puede obtenerse de diferentes maneras, incluyendo:
- Datos experimentales: Mediciones directas de presión y volumen durante un experimento.
- Ecuaciones de estado: Como la ecuación de estado de un gas ideal (PV=nRT), que relaciona la presión, el volumen, la cantidad de sustancia y la temperatura.
- Procesos termodinámicos específicos: Como procesos isobáricos (presión constante), isocóricos (volumen constante), isotérmicos (temperatura constante) o adiabáticos (sin intercambio de calor).
Una vez que se tiene la información necesaria, se grafican los puntos correspondientes a cada estado del proceso en el diagrama P-V. Luego, se unen estos puntos para obtener una curva que representa la trayectoria del proceso en el espacio P-V. La forma de esta curva dependerá del tipo de proceso termodinámico que se esté representando.
Ejemplos de procesos en un diagrama P-V:
- Proceso isobárico (Presión constante): Se representa como una línea horizontal en el diagrama P-V.
- Proceso isocórico (Volumen constante): Se representa como una línea vertical en el diagrama P-V.
- Proceso isotérmico (Temperatura constante): Para un gas ideal, se representa como una hipérbola (PV=constante).
- Proceso adiabático (Sin intercambio de calor): Se representa como una curva más pronunciada que la isoterma, ya que el cambio de presión es más significativo para un mismo cambio de volumen.
Interpretando Diagramas P-V: Trabajo y otras magnitudes
Los diagramas P-V son herramientas muy útiles para calcular el trabajo realizado por o sobre el sistema durante un proceso termodinámico. El trabajo (W) realizado por un gas en expansión se calcula como el área bajo la curva que representa el proceso en el diagrama P-V. Matemáticamente, se puede expresar como una integral:
W = ∫PdV
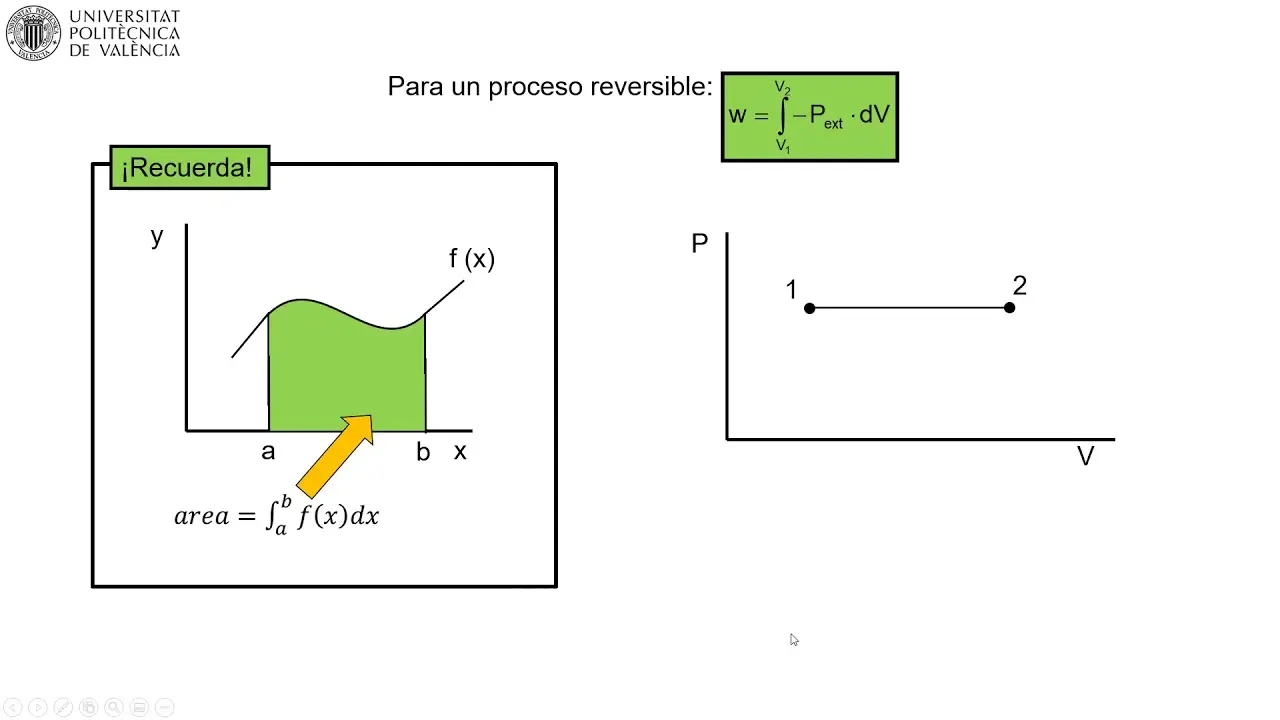
Donde la integral se calcula a lo largo de la trayectoria del proceso en el diagrama P-V. Para procesos sencillos, como los isobáricos, esta integral se simplifica al cálculo del área de un rectángulo. Para procesos más complejos, se pueden utilizar métodos de integración numérica.
Además del trabajo, los diagramas P-V también proporcionan información cualitativa sobre otros aspectos del sistema, como:
- Cambios en la energía interna: La forma de la curva en el diagrama P-V puede indicar si la energía interna del sistema aumenta o disminuye.
- Transferencia de calor: Combinando la información del diagrama P-V con la primera ley de la termodinámica (ΔU = Q - W), se puede determinar la cantidad de calor transferida durante el proceso.
- Reversibilidad e irreversibilidad: Un proceso reversible se representa por una curva continua y bien definida en el diagrama P-V, mientras que un proceso irreversible puede estar representado por una región más difusa.
Aplicaciones de los diagramas P-V
Los diagramas P-V tienen una amplia gama de aplicaciones en diferentes campos de la ciencia e ingeniería, incluyendo:

- Termodinámica de gases ideales y reales: Se utiliza para analizar el comportamiento de gases bajo diferentes condiciones.
- Motores de combustión interna: Se utilizan para modelar el ciclo de funcionamiento de motores de gasolina y diésel.
- Refrigeración y climatización: Se utilizan para analizar los ciclos de refrigeración y determinar la eficiencia de los sistemas.
- Ingeniería química: Se utilizan para el diseño y optimización de procesos químicos.
Consultas habituales sobre los diagramas P-V
Algunas consultas habituales que surgen al estudiar los diagramas P-V son:
- ¿Cómo se calcula el trabajo en un proceso cíclico? El trabajo en un proceso cíclico es igual al área encerrada por la curva que representa el ciclo en el diagrama P-V.
- ¿Qué significa una curva cerrada en un diagrama P-V? Una curva cerrada representa un proceso cíclico, donde el sistema regresa a su estado inicial después de una serie de transformaciones.
- ¿Cómo se diferencian los diagramas P-V para gases ideales y reales? Los gases ideales siguen la ecuación PV=nRT, mientras que los gases reales presentan desviaciones de este comportamiento, especialmente a altas presiones y bajas temperaturas. Estas desviaciones se reflejan en la forma de las curvas en el diagrama P-V.
- ¿Qué son las isotermas en un diagrama P-V? Las isotermas son líneas que representan procesos a temperatura constante. Para un gas ideal, son hipérbolas.
Tabla comparativa de procesos termodinámicos en un diagrama P-V
| Proceso | Descripción | Representación en el diagrama P-V |
|---|---|---|
| Isobaric | Presión constante | Línea horizontal |
| Isocórico | Volumen constante | Línea vertical |
| Isotérmico | Temperatura constante (Gas Ideal) | Hipérbola |
| Adiabático | Sin intercambio de calor | Curva más pronunciada que la isoterma |
En resumen, el diagrama P-V es una herramienta esencial en termodinámica que permite visualizar y analizar procesos termodinámicos, calcular el trabajo realizado y obtener información cualitativa sobre otras magnitudes termodinámicas. Su comprensión es fundamental para el estudio de diferentes sistemas físicos y sus aplicaciones en la ingeniería y la ciencia.

