19/08/2019
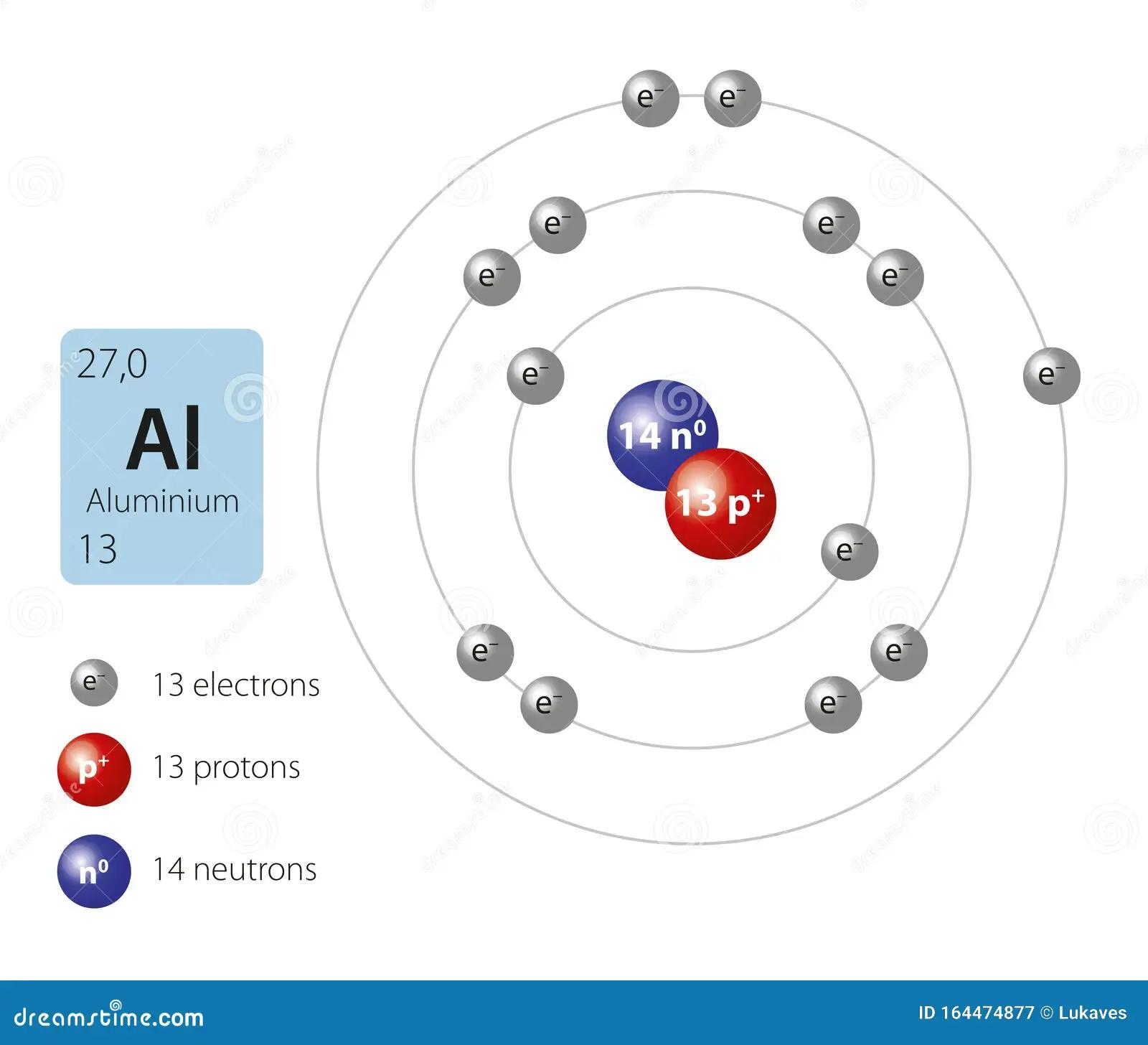
El aluminio, un elemento abundante y versátil, presenta una estructura atómica maravilloso que explica sus propiedades químicas y físicas. Si bien su estructura exterior (la nube de electrones) es compleja de representar visualmente con exactitud, la estructura interna del átomo de aluminio se puede comprender y graficar de manera simplificada, enfocándonos en el núcleo y la distribución de sus protones y neutrones.
Configuración electrónica y diagrama de orbitales
Para comprender la estructura interna del átomo de aluminio, debemos comenzar por su configuración electrónica. El aluminio tiene un número atómico de 13, lo que significa que posee 13 protones en su núcleo y, en estado neutro, 13 electrones orbitando alrededor. La configuración electrónica del aluminio es 1s²2s²2p⁶3s²3p¹. Esta configuración nos indica la distribución de los electrones en los diferentes niveles y subniveles de energía.
Podemos representar esta configuración mediante un diagrama de orbitales, que muestra visualmente cómo se distribuyen los electrones en los orbitales atómicos. Los orbitales s pueden contener hasta 2 electrones, mientras que los orbitales p pueden contener hasta 6 electrones. El diagrama de orbitales para el aluminio sería:
| Nivel de energía | Subnivel | Orbitales | Electrones |
|---|---|---|---|
| 1 | s | 1s | ↑↓ |
| 2 | s | 2s | ↑↓ |
| 2 | p | 2px 2py 2pz | ↑↓ ↑↓ ↑↓ |
| 3 | s | 3s | ↑↓ |
| 3 | p | 3px 3py 3pz | ↑ |
Este diagrama nos muestra que los dos primeros niveles de energía están completamente llenos, mientras que el tercer nivel de energía tiene un electrón desapareado en el subnivel p. Este electrón desapareado es el responsable de la reactividad química del aluminio.
El núcleo del átomo de aluminio
El núcleo del átomo de aluminio contiene 13 protones, partículas con carga positiva, y generalmente un número similar de neutrones, partículas sin carga. El número de neutrones puede variar, dando lugar a los diferentes isótopos del aluminio. La masa atómica del aluminio es aproximadamente 27 uma, que representa la suma de los protones y neutrones en el núcleo. La fuerza nuclear fuerte mantiene unidos a los protones y neutrones en el núcleo, a pesar de la repulsión electrostática entre los protones.
Representación gráfica simplificada
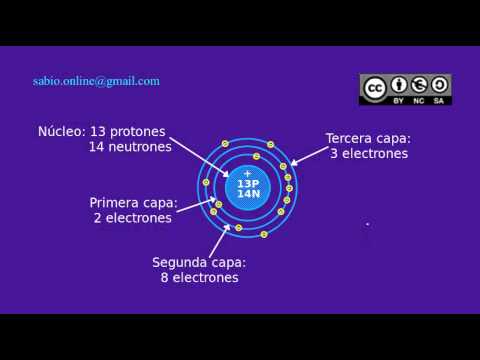
Para graficar la estructura interna del átomo de aluminio de forma simplificada, podemos representar el núcleo como una esfera pequeña y densa que contiene los 13 protones y los neutrones. Alrededor del núcleo, podemos representar las capas de electrones, aunque no a escala, ya que el tamaño real de los orbitales atómicos es mucho mayor que el tamaño del núcleo. Cada capa o nivel de energía contiene un cierto número de electrones, según la configuración electrónica. No intentaremos representar la forma y posición exactas de los orbitales, dado que es complejo y no aporta una visión intuitiva para este nivel de explicación.
Consultas habituales sobre la estructura del átomo de aluminio
Algunas de las consultas habituales sobre la estructura atómica del aluminio incluyen:
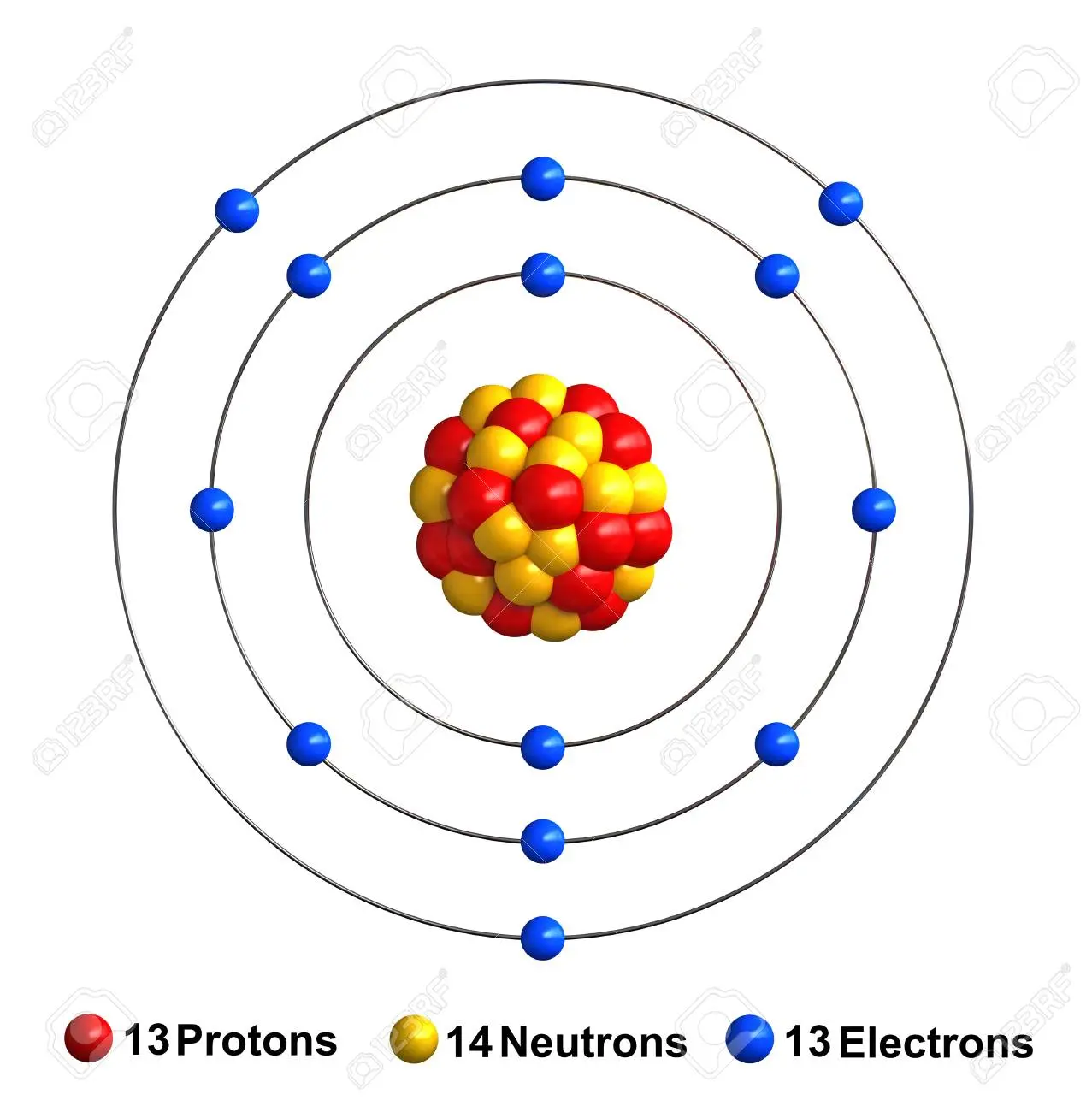
- ¿Cuántos protones tiene el aluminio? 13 protones.
- ¿Cuántos electrones tiene el aluminio en estado neutro? 13 electrones.
- ¿Cuál es la configuración electrónica del aluminio? 1s²2s²2p⁶3s²3p¹
- ¿Cuántos neutrones tiene un átomo de aluminio? Generalmente 14 neutrones (aunque existen isótopos con diferentes cantidades).
- ¿Por qué el aluminio es reactivo? Debido al electrón desapareado en su capa de valencia (3p¹).
- ¿Cómo se representa la estructura interna del átomo de aluminio? Mediante un modelo simplificado que muestra el núcleo con protones y neutrones, y las capas electrónicas con su respectiva cantidad de electrones.
Comparativa con otros átomos
Para comprender mejor la estructura del átomo de aluminio, podemos compararlo con otros átomos de elementos cercanos en la tabla periódica. Por ejemplo, el magnesio (número atómico 12) tiene una configuración electrónica 1s²2s²2p⁶3s², con dos electrones en su capa de valencia. El silicio (número atómico 14) tiene una configuración electrónica 1s²2s²2p⁶3s²3p², con cuatro electrones en su capa de valencia. Estas diferencias en la configuración electrónica explican las diferentes propiedades químicas de estos elementos.
| Elemento | Número atómico | Configuración electrónica | Electrones de valencia |
|---|---|---|---|
| Magnesio (Mg) | 12 | 1s²2s²2p⁶3s² | 2 |
| Aluminio (Al) | 13 | 1s²2s²2p⁶3s²3p¹ | 3 |
| Silicio (Si) | 14 | 1s²2s²2p⁶3s²3p² | 4 |
Consideraciones adicionales
Es importante recordar que el modelo atómico que hemos descrito es una simplificación. La mecánica cuántica proporciona una descripción más precisa y compleja de la estructura atómica, incluyendo la naturaleza probabilística de la posición de los electrones. Sin embargo, el modelo simplificado que hemos presentado es suficiente para comprender los aspectos fundamentales de la estructura interna del átomo de aluminio.
La representación gráfica del átomo de aluminio, enfocándose en su estructura interna, busca transmitir una idea clara de la distribución de protones, neutrones y electrones. Si bien no es posible una representación completamente exacta, el modelo simplificado permite comprender las bases de su comportamiento químico y físico.
Palabras clave: átomo de aluminio, estructura atómica, configuración electrónica, diagrama de orbitales, núcleo atómico, protones, neutrones, electrones, modelo atómico, tabla periódica, elementos químicos, representación gráfica, isótopos.