14/01/2018
El oxígeno, un elemento fundamental para la vida en la Tierra, presenta una estructura atómica maravilloso que merece ser explorada en detalle. A menudo, nos enfocamos en la fórmula química O₂, que representa la molécula de oxígeno diatómico presente en el aire que respiramos. Sin embargo, para comprender verdaderamente el comportamiento químico del oxígeno, es crucial analizar la estructura interna de su átomo individual, dejando de lado, por el momento, la representación de la molécula.
El Modelo Atómico y el Oxígeno
Para representar gráficamente la estructura interna del átomo de oxígeno, debemos recurrir a los modelos atómicos. Si bien existen varios modelos, el modelo mecánico cuántico proporciona la descripción más precisa y completa, aunque su complejidad visual lo hace menos accesible para una representación gráfica simple. A menudo, se utiliza una representación simplificada, que se basa en la distribución de los electrones en los niveles de energía o capas electrónicas.
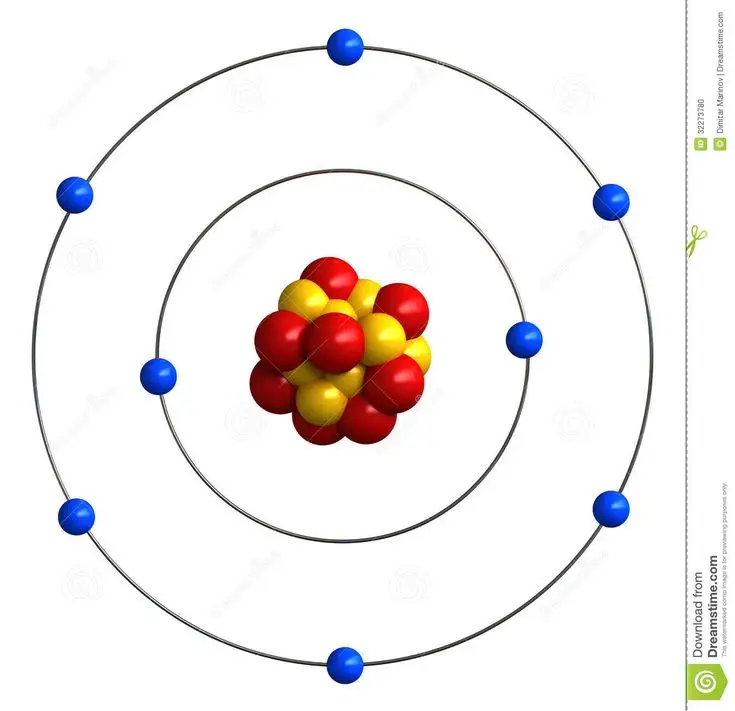
El átomo de oxígeno (O) tiene un número atómico de 8, lo que significa que posee 8 protones en su núcleo y 8 electrones orbitando alrededor de él en estado neutro. La disposición de estos electrones determina las propiedades químicas del oxígeno.
Configuración Electrónica y Representación
La configuración electrónica del oxígeno es 1s²2s²2p⁴. Esta notación indica la distribución de los electrones en los diferentes niveles de energía:
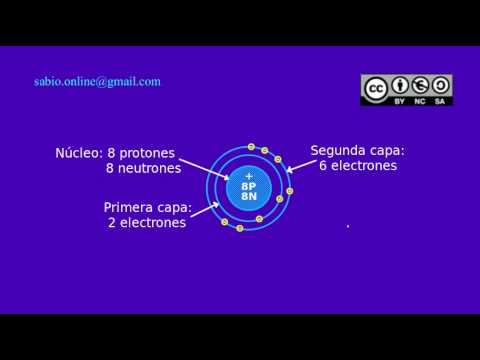
- Nivel de energía 1 (capa K): Contiene 2 electrones en el subnivel 1s.
- Nivel de energía 2 (capa L): Contiene 6 electrones, 2 en el subnivel 2s y 4 en el subnivel 2p.
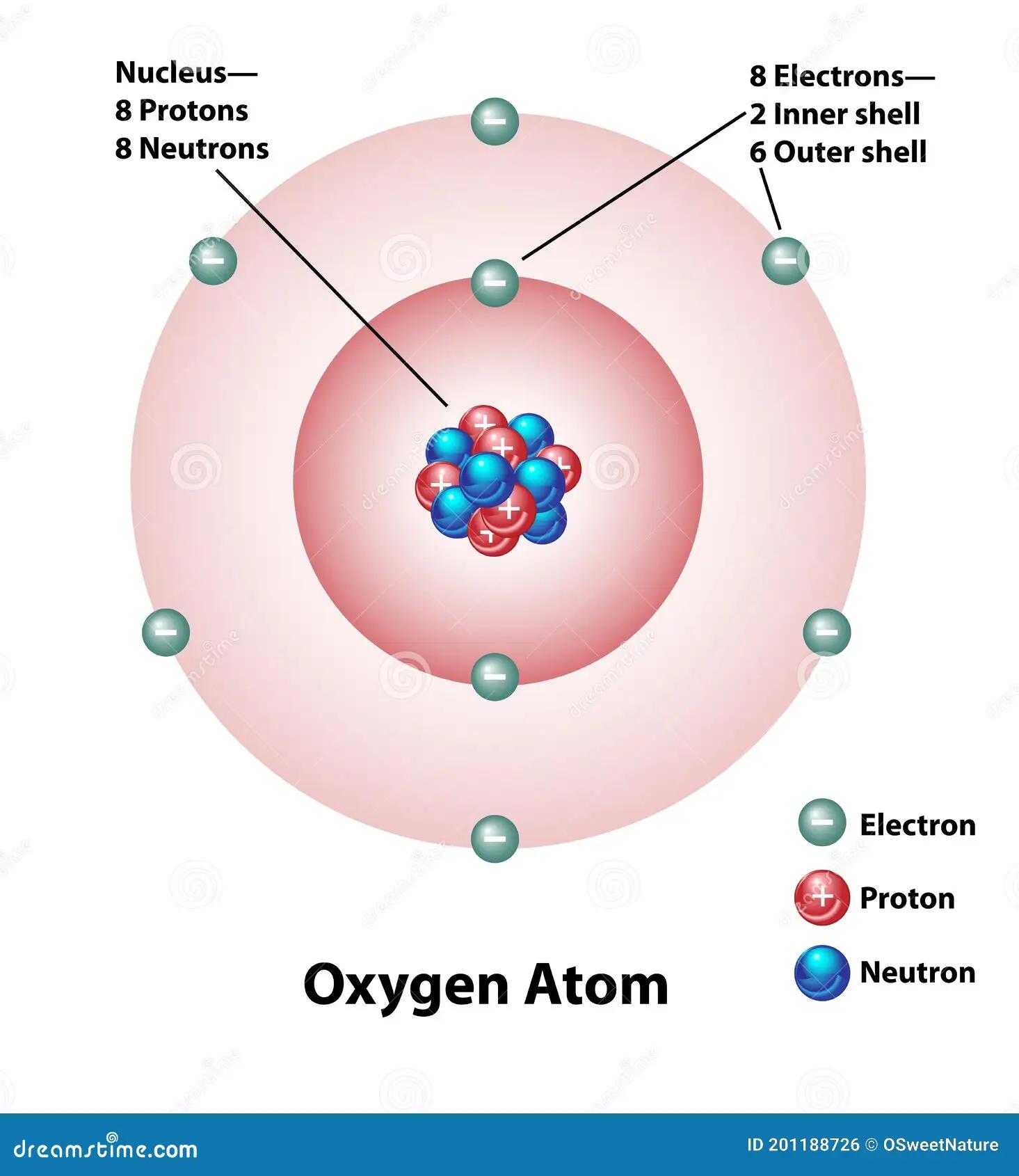
Para una representación gráfica simplificada, podemos visualizar el núcleo (con 8 protones y 8 neutrones) en el centro, rodeado por dos capas de electrones. La capa interna (K) contiene 2 electrones, mientras que la capa externa (L) contiene los 6 electrones restantes. Es importante recordar que esta es una simplificación; los electrones no orbitan en trayectorias definidas como los planetas alrededor del sol, sino que ocupan orbitales atómicos con diferentes formas y energías.
Orbitales atómicos y la capa de valencia
Los 4 electrones del subnivel 2p se distribuyen en tres orbitales (2px, 2py, 2pz), con un máximo de dos electrones por orbital. Dos de estos orbitales estarán llenos y dos contendrán un electrón cada uno. Esta configuración de la capa de valencia (la capa externa de electrones) es crucial para la reactividad química del oxígeno. La capacidad de compartir o ganar electrones para completar su octeto (8 electrones en la capa de valencia) explica la alta reactividad del oxígeno y su tendencia a formar enlaces químicos.
Comparación con otros átomos
| Átomo | Número Atómico | Configuración Electrónica | Electrones de Valencia |
|---|---|---|---|
| Oxígeno (O) | 8 | 1s²2s²2p⁴ | 6 |
| Nitrógeno (N) | 7 | 1s²2s²2p³ | 5 |
| Carbono (C) | 6 | 1s²2s²2p² | 4 |
| Flúor (F) | 9 | 1s²2s²2p⁵ | 7 |
Esta tabla muestra la configuración electrónica y el número de electrones de valencia de algunos elementos cercanos al oxígeno en la tabla periódica. La comparación permite observar las diferencias en la configuración electrónica y cómo esto afecta a la reactividad química de cada elemento.
Consultas habituales sobre la representación del átomo de oxígeno
A continuación, se responden algunas de las consultas más frecuentes sobre la representación del átomo de oxígeno:
- ¿Por qué el oxígeno es tan reactivo? Su alta reactividad se debe a su configuración electrónica, con 6 electrones de valencia, lo que lo hace propenso a ganar o compartir dos electrones para completar su octeto y alcanzar una configuración estable.
- ¿Cómo se representa la molécula de O₂? La molécula de oxígeno (O₂) se representa mediante un doble enlace entre dos átomos de oxígeno, cada uno compartiendo dos electrones para completar su octeto.
- ¿Qué es la capa de valencia? La capa de valencia es la capa electrónica más externa de un átomo, y sus electrones son los responsables de las propiedades químicas del elemento.
- ¿Qué significa la configuración electrónica? La configuración electrónica describe la distribución de los electrones en los diferentes niveles y subniveles de energía de un átomo.
Conclusión
La representación gráfica del átomo de oxígeno, aunque simplificada, nos permite comprender su estructura interna y cómo esta estructura determina sus propiedades químicas. La configuración electrónica, con sus 6 electrones de valencia, explica la alta reactividad del oxígeno y su importancia en diversos procesos químicos y biológicos. Si bien el modelo mecánico cuántico ofrece una descripción más precisa, las representaciones simplificadas son esenciales para una comprensión inicial de este elemento crucial para la vida.
Palabras clave: átomo de oxígeno, representación gráfica, configuración electrónica, capa de valencia, estructura atómica, modelo atómico, electrones, protones, neutrones, orbitales atómicos, reactividad química, estequiometría.